3D打印生物可吸收血管支架的两段式降解及促进功能性新生内膜的特性(2)
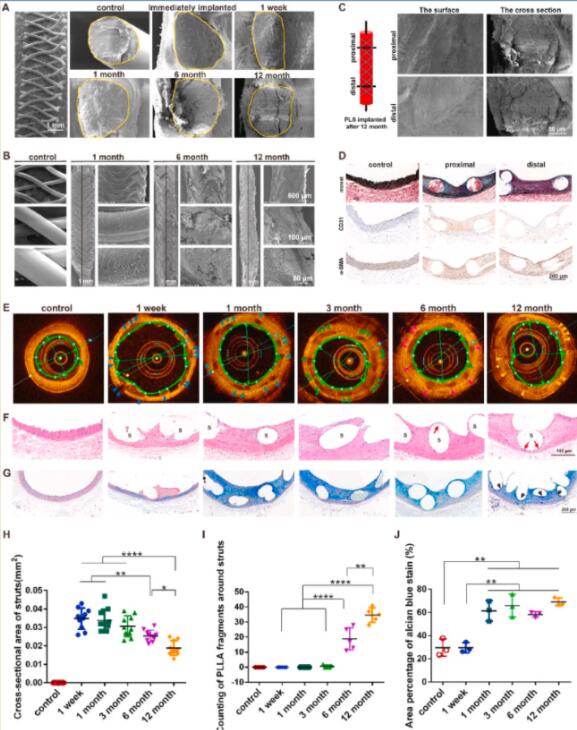
聚乳酸生物可吸收血管支架植入大鼠腹主动脉6个月后,支架丝的降解显著,伴随着支架的显著降解,支架段及其近、远心端力学环境发生显著改变。特别是在12个月时近、远心端胶原等ECM的沉积产生显著差异,进一步佐证了血管组织对降解引起的力学环境动态变化有显著的响应,同时也对支架的降解产生影响,而使支架远心端的降解明显强于近心端(图3)。
聚乳酸生物可吸收血管支架降解吸收后对血管壁的力学刺激逐渐降低
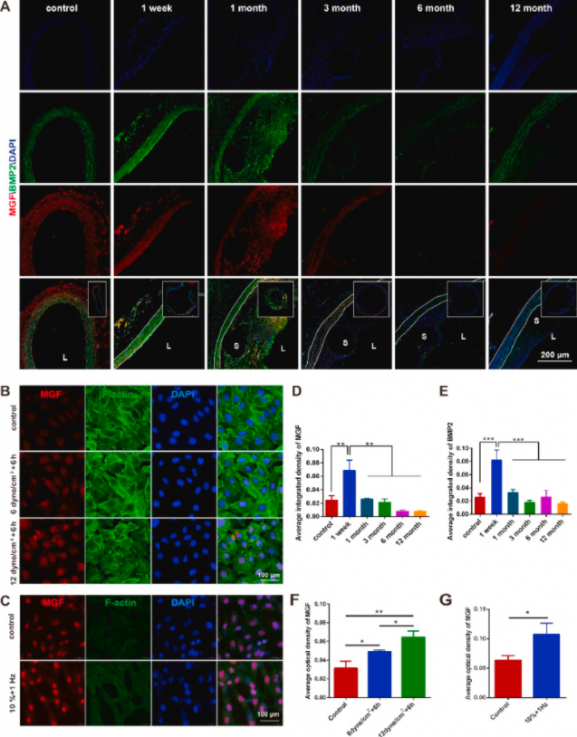
聚乳酸生物可吸收血管支架降解引起的力学性能变化,是其功能发挥的关键。我们以血管局部力生长因子(表达量与力学刺激强度呈正相关)表达量的动态变化来反应由支架降解产生的力学微环境变化。随着支架的降解,力生长因子随时间延长其表达量下调,表明支架对血管壁的力学刺激逐渐下降,有利于内皮的修复和抑制内膜的增生(图4)。
聚乳酸生物可吸收血管支架逐渐降解吸收后的血管正性重构
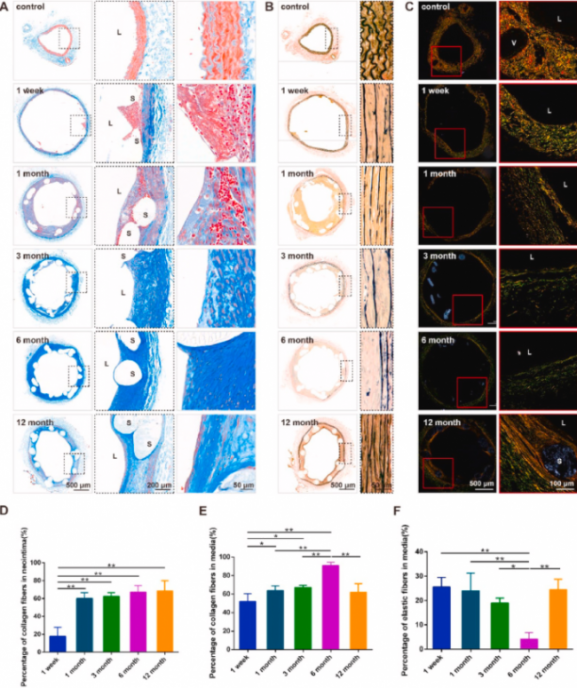
聚乳酸生物可吸收血管支架的降解,可消除植入物对血管壁的刺激,从而使血管发生正性重构,血管的弹性和舒缩功能逐渐恢复。我们的结果显示,支架植入会刺激胶原增生,同时伴随弹性纤维的减少。但是6个月后,管壁的胶原减少,弹性纤维增加,到12个月时,血管中膜的胞外基质成分可恢复到植入前水平,预示着血管良好的正性重构,弹性和舒缩功能恢复(图5)。
因此,该研究表明,在大鼠腹主动脉内3D打印生物可吸收支架具有比金属支架更快速的功能性内皮修复和血管正性重构,辅以个性化的复合药物涂层设计,结合生物可吸收支架的重复介入治疗和与磁共振检查兼容等优势,相信新一代的生物可吸收支架能够使更多的患者获益。
注:PLS : poly-l-actide vascular scaffolds,聚乳酸血管支架。
l 作者信息
第一作者/通讯作者:尹铁英
博士,重庆大学生物工程学院副教授,博士生导师。
通讯作者:王亚洲
中美联合培养博士,教授/博导,重庆大学医学院副院长。
通讯作者:王贵学
博士,教授/博导。连续3年(2019-2021)入选爱思唯尔中国高被引学者和全球顶尖前10万科学家榜单。
(责任编辑:admin)


 CNES引入INTAMSYS聚合物FF
CNES引入INTAMSYS聚合物FF 具有显著纵波传播特性的三
具有显著纵波传播特性的三 生物3D打印、类器官应用,
生物3D打印、类器官应用, MIT新突破:无需半导体也
MIT新突破:无需半导体也 亚马逊和Holcim投资14Tree
亚马逊和Holcim投资14Tree 回收SLS 3D打印尼龙废料,
回收SLS 3D打印尼龙废料, 《Small Science
《Small Science 南洋理工-剑桥大
南洋理工-剑桥大 清华大学:抗拉强
清华大学:抗拉强 《Science》:一
《Science》:一 国产大尺寸陶瓷3D
国产大尺寸陶瓷3D 南京工业大学:基
南京工业大学:基

