华盛顿大学Kelly R. Stevens教授团队在Nature Reviews Materials|跨尺度血管网络
时间:2022-10-24 13:14 来源:南极熊 作者:admin 阅读:次

血管网络的发生和特征
在胚胎发育过程中,当来自血岛的成血管细胞群分化为内皮细胞并形成内部通道(管腔)时,血管网络就会出现,然后相互吻合形成一个连接的分支网络,称为原始血管丛。这种内皮细胞的合并和自我组装被称为血管发生(vasculogenesis)。然后,原始血管丛重塑以满足代谢需求,具体方式为新的血管从具有高氧需求的组织中的现有血管中萌发,这一过程被称为血管新生(angiogenesis)。血管发生(vasculogenesis)和血管新生(angiogenesis)通称为新血管化(neovascularization)。血管丛的重塑使血管网络更有效率,一些血管合并和扩大,一些减少。随后在分子信号和血液动力相互作用下,血管网络逐渐成熟,其最突出特征是:结构和细胞水平的不同血管层次形成。
血管生成完毕后,高代谢的实体组织和器官中的血管层次分为大血管(动脉和静脉, 0.1-10.0 mm)和适配微血管循环的小血管(小动脉,小静脉和毛细血管, 8-100 μm)。一般来说,大动脉和静脉负责输送血液进出心脏,它们有三个结构独特的拥有属性: 内皮化内层、肌肉中层和胶原外(支持)层。随后,血液进入小动脉进行微血管循环,完成总外周阻力调节。与动脉类似,小动脉也有三层,但厚度较小。总外周阻力由动脉和小动脉的肌肉层调节,收缩和扩张以匹配氧气输送速率和组织需求。随后血液随着小动脉进入毛细血管,通过单层内皮细胞壁与周围细胞发生气体交换。缺氧和富含二氧化碳的血液进入毛细血管后流入小静脉,这种小静脉类似于小动脉,但是具有较薄的壁和弹性较小的组织。最后,血液进入大静脉,最终回到心脏。
在胚胎发育过程中,当来自血岛的成血管细胞群分化为内皮细胞并形成内部通道(管腔)时,血管网络就会出现,然后相互吻合形成一个连接的分支网络,称为原始血管丛。这种内皮细胞的合并和自我组装被称为血管发生(vasculogenesis)。然后,原始血管丛重塑以满足代谢需求,具体方式为新的血管从具有高氧需求的组织中的现有血管中萌发,这一过程被称为血管新生(angiogenesis)。血管发生(vasculogenesis)和血管新生(angiogenesis)通称为新血管化(neovascularization)。血管丛的重塑使血管网络更有效率,一些血管合并和扩大,一些减少。随后在分子信号和血液动力相互作用下,血管网络逐渐成熟,其最突出特征是:结构和细胞水平的不同血管层次形成。
血管生成完毕后,高代谢的实体组织和器官中的血管层次分为大血管(动脉和静脉, 0.1-10.0 mm)和适配微血管循环的小血管(小动脉,小静脉和毛细血管, 8-100 μm)。一般来说,大动脉和静脉负责输送血液进出心脏,它们有三个结构独特的拥有属性: 内皮化内层、肌肉中层和胶原外(支持)层。随后,血液进入小动脉进行微血管循环,完成总外周阻力调节。与动脉类似,小动脉也有三层,但厚度较小。总外周阻力由动脉和小动脉的肌肉层调节,收缩和扩张以匹配氧气输送速率和组织需求。随后血液随着小动脉进入毛细血管,通过单层内皮细胞壁与周围细胞发生气体交换。缺氧和富含二氧化碳的血液进入毛细血管后流入小静脉,这种小静脉类似于小动脉,但是具有较薄的壁和弹性较小的组织。最后,血液进入大静脉,最终回到心脏。
工程化方法构筑血管网络
1. 微型制造
微型制造方法能够创建相对复杂的可灌注微流体网络。主流方法为将光刻胶在硅片上图案化以创建微通道管腔的拓扑特征,然后使用聚(二甲基硅氧烷)(PDMS)倒模产生可灌注微通道,模拟分支血管样网络,这种方法能够复制血管拓扑的某些特征(连通性和几何形状) 。然而,PDMS 是一种合成材料,不能提供在天然血管基质环境,并且不支持周围组织(实质细胞)或功能细胞的包裹。因此,部分研究在PDMS中创建了血管网络图案并将其作为模具在更具生物相容性的材料中创建微模制通道。
微型制造方法的主要限制是拓扑结构只能二维制作平面上制造缺少三维结构。为了克服这个限制,有研究使用逐层叠加的制造三维结构 (图1b)。该方法中首先利用微型制造方法得到微道通然后堆叠,对齐和层压形再次成型。已有研究借助此方法组装了具有完整血管样网络的心脏组织,该网络的入口和出口通道成功连接了大鼠股动脉和静脉。
2. 激光降解与生物打印
为了克服微型制造的设计限制,激光降解和生物打印直接制造三维血管网络。
在激光降解方法中,激光通过光栅作用于材料上,以局部空间降解水凝胶形成三维血管网络。结合多光子显微镜,这种技术将局部降解限制在空间中的单一点,使用户能够“书写”复杂和精确的含曲率特征的毛细管尺度三维微通道网络(图1c)。这种方法已经被用于制造直径小至5μm 的通道,这是人体中已知的最小血管的尺寸。这些微通道可以引导内皮细胞长入形成毛细血管。虽然激光降解对于构建相对较小的目标区域是有价值的,但是仅使用这种技术产生大血管梯度血管结构仍然是不可能的。
鉴于创建更大体积组织的需求,3D打印凭借其快速制造空间血管网络的潜力受到越来越多的关注 (图1d)。然而,由于打印分辨率和挤压时对细胞的剪切损伤的限制,这种技术无法完成精细血管网络的打印。针对于这一问题,研究人员开发了打印“牺牲”材料的策略,创建血管网络结构后将其嵌入更大的水凝胶中,细胞被包裹在大块的水凝胶中,而不是打印的血管网络结构,之后将牺牲材料溶解以形成微流体血管网络,管道内壁也可以进行细胞接种。常见的牺牲墨水包括基于碳水化合物的玻璃, Pluronic F127和明胶,这些材料都兼顾了可打印性、打印分辨率和3D 血管拓扑结构的复杂性。挤出生物打印的有限分辨率阻碍了其应用于制造小于大小动脉(约200 μm)的管道。
研究人员颇具创造性的优化了上述牺牲模板法,提出了名为FRESH的任意将打印材料挤入悬浮自愈水凝胶的打印方法,实质为生物墨水在可溶性明胶支持浴完成挤出打印。第二代版本FRESH 2.0能够打印直径小至20μm 的无细胞胶原管腔结构。该技术已被用于制造可灌注的多尺度血管网络,以模拟冠状动脉血管,管腔直径小至100μm。尽管这在无细胞挤出生物打印的分辨率方面是一个相当大的飞跃,但是直接打印细胞仍然需要大得多的喷嘴尺寸(大约是细胞直径的10倍),因此分辨率仍然较低。此外,挤出打印用于血管网络形成的另一挑战是,较低的打印效率。虽然新兴技术可能最终解决这一限制,但目前需要在制造时间和组织体积之间进行权衡。
立体光刻(SLA)打印提供了一种完全不同的生物打印方法,为大体积制造提供了额外的优势。通过在可光聚合的水凝胶前驱体内投射 x-y 平面光,SLA 打印机可以一个平面一个平面地制造结构从而快速构建实体。SLA 用于生物打印最初受到了光穿透性过强通过多个打印层的限制,这阻止了空间血管网络特征和许多拓扑细节的打印。为了解决这一问题,生物相容性食品安全染料被添加到预聚物浴中以限制光的穿透,使得打印成千上万层具有复杂拓扑结构的可灌注血管网络成为可能。SLA 打印已被用于模拟相互关联肺泡的3D 结构和工程肝组织的分支管状网络构建,证明了该方法可以复现复杂的自然拓扑的能力。然而,尽管在血管拓扑结构的制作方面取得了相当大的进展,这种方法目前仍然局限于300μm打印分辨率。
诸如激光降解和生物打印等实体制造方法的进展使我们更接近于在“3D 打印器官”内制造血管网络的可能性。尽管每种技术仍然需要在材料、分辨率、打印时间或打印结构尺寸方面进行权衡,但这些技术有望与器官芯片技术结合,进一步形成多尺度血管网络。
3. 材料学考量
各种工程技术中所使用材料的生物相容性是制备血管网络的一个重要考虑因素。这些材料课根据它们是天然来源还是合成水凝胶进行分类,现多用混合材料发挥两者不同优势。
天然基质材料如胶原蛋白、纤维蛋白、脱细胞细胞外间质(ECM)或基质胶提供细胞粘附位点,含有天然信号传导能力,并可被细胞过程降解以允许水凝胶重塑,微型制造和挤压生物打印已被用于在一些天然基质中创建可灌注血管。值得注意的是,材料特性决定了天然聚合物与每种技术的兼容性,例如,微型制造技术要求材料在移除模具后的工艺和培养过程中能承受一定的压力或剪切力保持拓扑特征。因此,较硬的材料(弹性模量较高的材料)更常用于微型制造(例如 > 10mg/ml纤维蛋白或5-6mg/ml胶原蛋白)。类似地,可打印性与保真度影响挤出打印材料的选择,需考虑的参数主要包括材料的粘度、弹性恢复和剪切应力下的流变行为。许多用于挤出打印的材料要么天然具有剪切变稀特性,要么被改性使其具有剪切变稀特性。这样当材料穿过打印喷嘴时,其粘度在剪切应力作用下降低。相反地,基于光的血管网络制造方法,如层层光刻、多光子激光消融和 SLA 生物打印要求材料具有光活性。因此,主要是合成聚合物适配这些技术。例如,早期的光刻领域使用具有光交联基团的合成聚乙二醇基材料,如聚乙二醇二丙烯酸酯(PEGDA)。当在光引发剂存在下暴露于光下时,这些材料形成共价交联。光引发剂的选择和浓度对材料的细胞相容性和细胞存活至关重要。尽管 PEGDA 和类似的合成聚合物具有光活性,但它们缺乏天然 ECM 提供的生物活性信号,因此不能很好地支持工程血管网络中的活细胞存活。为了解决这一缺陷,材料科学家将合成聚合物功能化,使其包括一些天然的 ECM 特征,具体包括添加酶降解连接和肽部分,如 Arg-Gly-Asp (RGD)细胞粘附识别信号。在合成材料中结合生物活性分子有助于不同细胞群的存活,功能实现和重塑,包括排列成血管的内皮细胞和支撑它们的壁细胞。
其他一些研究还对天然材料进行了改性,以引入与合成材料有关的非天然控制特征,例如光活性,使其与各种生物制造策略兼容。例如,为了使天然材料明胶具有光活性,可以用甲基丙烯酸酯基团修饰明胶大分子来制备明胶甲基丙烯酸酯(GelMA)。当在光引发剂存在下暴露于光下时,GelMA 聚合形成交联的水凝胶。
新型材料对于工程血管网络的许多技术进步至关重要。通常,这些材料已经从其他行业,如食品工业,被借鉴的用于组织工程。这包括明胶的引入,明胶是由胶原蛋白的三螺旋结构的部分分解产生的,最初是肉类加工业的副产品。从食品工业采用的其他材料的例子包括用于3D 打印牺牲血管网络的碳水化合物玻璃(例如糖制剂)以及向水凝胶前体添加食品安全染料以阻止多层 SLA 打印中不需要的(平面外)光的传输。
尽管取得了一些突破性的技术进步,但工程驱动的方法技术仍然无法复制自然血管网络。主要瓶颈在于无法从细胞和分子水平上复制血管层次结构。目前,大多数工程化的血管网络只包含一个单一的内皮细胞群,这些内皮细胞在通道的内表面形成一个单一的汇合层。虽然一些研究小组已经在血管通道周围的基质中添加了基质细胞或周细胞,但是还没有形成控制血管张力的血管周膜。新材料将继续推动工程驱动的血管网络构建的发展,同时,为了在细胞层面构建血管网络,部分研究采取了一种完全不同的方法即通过自然驱动构建血管网络。
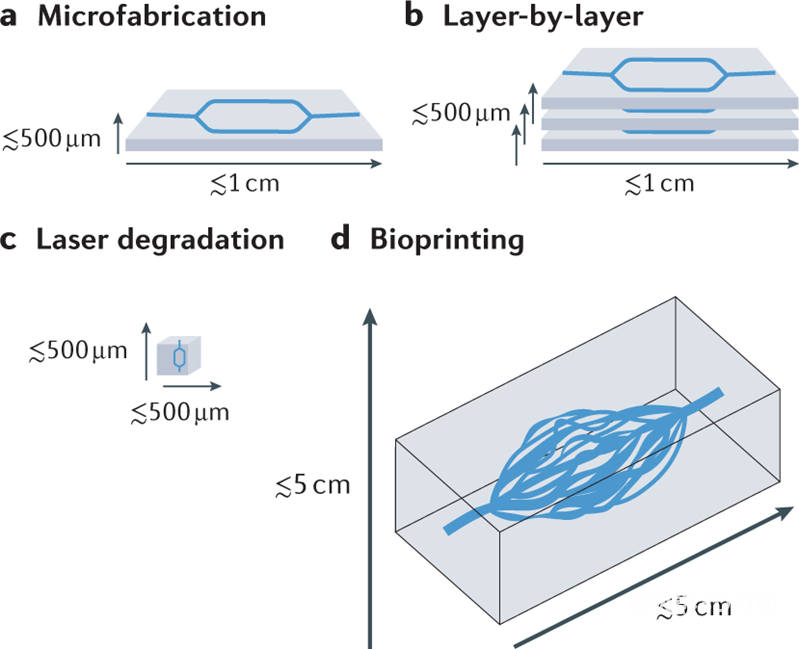
图1.(a)微型制造能够在微尺度上排列细胞和材料,在薄的成型平面上创建复杂的可灌注微流体网络。(b)微型制造的单层网络可以层层叠加、对齐以增加组织厚度。(c)激光降解使用多光子显微镜等工具来局部降解光敏水凝胶,使用户能够“书写”复杂和精确的管腔尺寸近似于毛细血管的3D微通道网络。(d)生物打印能够以比激光降解更大的规模、速度、体积制造血管网络,但分辨率较低。
生物驱动方法构筑血管网络
1. 自组装血管网络
与工程驱动的方法相反,生物驱动的方法依赖于细胞群落经历形态发生和自组装成血管网络的固有能力。1988年,研究人员观察到在3D 层粘连蛋白和胶原基质中培养的内皮细胞具有在体外自组装成血管样网络的能力。从那时起,其他基质,包括纤维蛋白,胶原和透明质酸水凝胶,也被证明可以支持内皮细胞自组装成血管样网络。值得注意的是,这个过程也可以通过将内皮细胞接种在天然材料(纤连蛋白和胶原蛋白)中,或合成材料上(聚(乳酸-羟基乙酸)(PLGA)和聚(L- 乳酸)(PLLA))并植入免疫缺陷小鼠中。所得到的自组装内皮网络与宿主血管吻合,形成内部血液灌流。
尽管早期的研究证明了细胞自我组装的潜在力量,但是仅来自内皮细胞的血管是不稳定的,并且随着时间的推移容易消退。通过平滑肌细胞或周细胞与内皮细胞的结合可形成稳定的天然血管,并且类似地,血管周支持细胞可以使体内植入的工程化血管网络呈现稳态。在纤维连接蛋白和胶原支架中共同接种间充质细胞和内皮细胞能够在支架植入后形成稳定灌注的移植物来源的血管。基质细胞还支持甚至增强血管网络在体外和植入其他材料环境中的自组装,如在纤维蛋白或 PLGA 和 PLLA 水凝胶中,甚至在“无支架”的情况下,血管网络也可以在仅由细胞和这些细胞分泌的基质组成的实体中萌发。包含基质细胞支持的自组装血管网络也被用于支持实质细胞用于多种器官的制造,包括用于骨骼肌,心脏和肝组织工程。
在过去的十年中,自组装领域已经将重点转向通过结合微环境因素(如控制灌注)在体外创建更具生理相似性的血管网络。这项工作的大部分在微流体平台中进行,例如,在微流控芯片中将血管生成生长因子或基质细胞与内皮细胞结合可诱导内皮发芽或自组装以产生具有显著通道的稳定和可灌注的血管网络。血管丛的形成可以通过瞬时重新激活与内皮细胞中胎儿细胞状态相关的转录因子来增强,然后将其纳入微流控平台。这些模型已被用于筛选疾病(包括癌症) 治疗策略,并用于构建穿透高度选择性的血脑屏障模型。
2. 类器官
利用自组装原理的一个新兴领域是创建血管化类器官,即直径约为150μm 的3D迷你器官,复制了真实生物体的发育,结构和功能特性。许多器官(如肝脏,胰腺和肺)在胚胎发育中的器官发生过程中与血管化类器官相似。大多数体外血管化类器官的采取了将内皮细胞与器官特异性细胞混合的共培养方法或使用可以在类器官成熟过程中分化成各种血管细胞类型的中胚层前体的共分化方法。尽管这两种方法都能够在类器官培养过程中形成内皮管状网络,但这些围绕类器官的自组装网络的体外灌注仍然具有挑战性。多个研究小组已经证明,这些“血管化”类器官的体内植入导致预先组装的血管网络的快速灌注和类器官的进一步成熟。
大多数创建自组装网络的方法产生的血管大小范围从毛细血管到小动脉尺度(直径5-50μm)。通过该方法产生多层次的血管结构层次仍然具有挑战性。但有研究表明这种结构限制可以通过创造血管类器官来克服。血管类器官是在体外由人工多能干细胞(iPSC)衍生的内皮细胞产生的(图2b)。在植入免疫缺陷小鼠的肾囊时,这些类器官在体内自组装形成一个包括动脉、小动脉、小静脉和毛细血管的灌注分层网络。这种方法的成功表明,基于血管类器官的自组织系统具有复制跨尺度血光网络的潜力。由于上述研究是将将组织植入体内以自组装形成完全成熟的血管网络,如何在体外重现并阐明这些线索将是构建具有血管层次结构的血管化系统的主要步骤。
由人类血管类器官创造的血管网络可为疾病建模和药物筛选提供新的机会。这种类器官已被用于鉴定糖尿病和 SARS-CoV-2感染的新疗法。在这两个例子中,血管类器官复现了人类疾病的特征,并被用于测试未来临床使用的潜在药物。
3. 材料学考量
在随机分散的内皮细胞悬浮液和类器官内,选择支架材料来包埋内皮细胞对于帮助血管网络的自组装是必不可少的。与工程驱动的方法相反,该领域早期使用的大多数基质来自天然聚合物,如 Matrigel、纤维蛋白和胶原蛋白。这种天然聚合物的主要优点是含有粘合配体并具有重塑能力,共同支持血管发生和自组装。
尽管天然水凝胶具有生物学上的优势,但它们很难制备,而且易受到天然批次变化的影响。具体而言,类器官的培养经常依赖于基质胶,这是一种来自小鼠肿瘤细胞的化学成分不明的 ECM 混合物。此外,许多天然聚合物的复杂性使其化学或机械改性难以进行,限制了进一步调整这些材料以提高性能的能力。然而,天然材料仍然有很大的用途,在当下仍然是用于血管自组装的常规材料。
为了应对天然材料的一些缺陷,一些研究小组已经开发出合成或混合材料,模拟了天然基质的一些血管生成特征。例如,以透明质酸为基础的水凝胶可调和独特的合成环境,结合可溶性血管生成因子,能促进人类胚胎干细胞的血管分化。随后的研究表明,通过将多能干细胞包埋至透明质酸水凝胶内,成功地分化形成血管网络。
工程组织中基质的弹性模量也影响细胞行为,包括内皮细胞的自组装。常用于调节水凝胶刚度的方法是依赖于增加基质浓度,尽管使用这种方法时刚度和材料密度都发生了显著的变化。有趣的是,增加基质浓度会抑制3D 水凝胶中的内皮萌发,而增加与密度无关的刚度则有相反的效果。该结果表明,隔离材料刚度与其他因素对血管网络的影响需要进一步研究。除了对血管发生行为的影响,调整基质刚度也可以改善血管结构的控制。例如,改变与孔径或材料浓度无关的基质硬度可以控制胶原凝胶中自组装血管的管腔大小。硬凝胶(20,000 Pa)促进更大的多细胞腔形成,而软凝胶(5,000 Pa)诱导致密的薄血管网络。
一个有趣的发展方向是动态水凝胶,其可以迅速改变其粘弹性质以响应由包裹细胞引发的牵引力,从而模仿天然组织的机械敏感性。这些响应细胞行为的动态水凝胶通过促进诱导收缩的整联蛋白聚集,帮助在体外和体内形成自组装的血管网络,这些发现暗示了细胞与其细胞外环境之间双向通信的重要性。
尽管大量研究确定了较为合适的材料以支持血管网络形成,但是细胞自身的分泌作用也同样重要,细胞可以分泌基质分子和修饰剂,随着时间的推移降解和取代合成或天然基质。因此,最初的基质材料将在不刻意控制的情况下发生变化,细胞本身也会发生不同。工程自组装血管网络的未来发展除了需要提供适当的生物化学线索外,也应调整其物理和化学性质以响应细胞行为来实现细胞-ECM 通信。

图2.(a)自然驱动的方法依赖于细胞群落进行形态发生的固有能力(即导致细胞或组织发展其特征形状的生物学过程)并自组装成血管网络。例如,内皮细胞和基质细胞的共培养可以自发地自组装成血管网络。(b)一种由人工多能干细胞来源的内皮细胞在体外自组装形成的血管类器官。植入小鼠体内后,这些类器官在体内进行重塑,形成灌注的跨尺度血管网络。
参考文献
O’Connor C, Brady E, Zheng Y, et al. Engineering the multiscale complexity of vascular networks[J]. Nature Reviews Materials, 2022: 1-15. https://doi.org/10.1038/s41578-022-00447-8
(责任编辑:admin)
最新内容
热点内容


 适配多类别高温聚合物FFF
适配多类别高温聚合物FFF 埃肯与Startuplab合作加速
埃肯与Startuplab合作加速 NAMIC 全球增材制造峰会GA
NAMIC 全球增材制造峰会GA 3iD率先引进全新粘结剂喷
3iD率先引进全新粘结剂喷 Freeform人工智能3D打印工
Freeform人工智能3D打印工 Biomaterials science:牛
Biomaterials science:牛 卡内基梅隆研究人
卡内基梅隆研究人 Align Technology
Align Technology AM Craft在种子轮
AM Craft在种子轮 Aerojet拿下五角
Aerojet拿下五角 印度初创公司在Gi
印度初创公司在Gi 美军使用金属3D打
美军使用金属3D打

