3D��ӡ�������ײ���֧��
ʱ�䣺2020-02-24 16:12 ��Դ���ϼ��� ���ߣ��й�3D��ӡ�� �Ķ�����
�������ף�Fn����Ϊһ����Ϊ��Ҫ��ϸ������ʣ�ECM�����ף�������2ά����3ά��ϸ������ϵͳ�У�����ΪͿ��������һ���ܹ�֧��ϸ�����Ļ��������ǣ���Щ����Ϳ���Ϳ����ʽ��������ϸ�������������������ECM��Fn����Ľṹ���ܲ�һ�¡����ڣ�������������ѧ��Joerg Lahann�����Ŷ���Advanced Materials��־�Ϸ�������ΪEngineered Fibrillar Fibronectin Networks as Three-Dimensional Tissue Scaffolds�����£�������һ��������״�ۺ���֧��֧�ţ���ϸ������ѧ���ܺã��ҳ߶ȿɿص�3ά��ά�������ף�fFn�����硣����ͨ���ڿ�����Fn��Һ������֧�ܵ�3�ཻ�紦��ͨ��ˮ�����յ��ķ�ʽ�������γ�ʮ���ȶ���fFn���硣��fFn������Դٽ�ϸ����������ֳ��������������ԭ����ϸ�����յ������ת����δ����������fFn��������Ӧ���ڻ���ϸ���о�����ҽ�ƣ�ҩ����Ժ��ٴ�ǰ��ϡ�
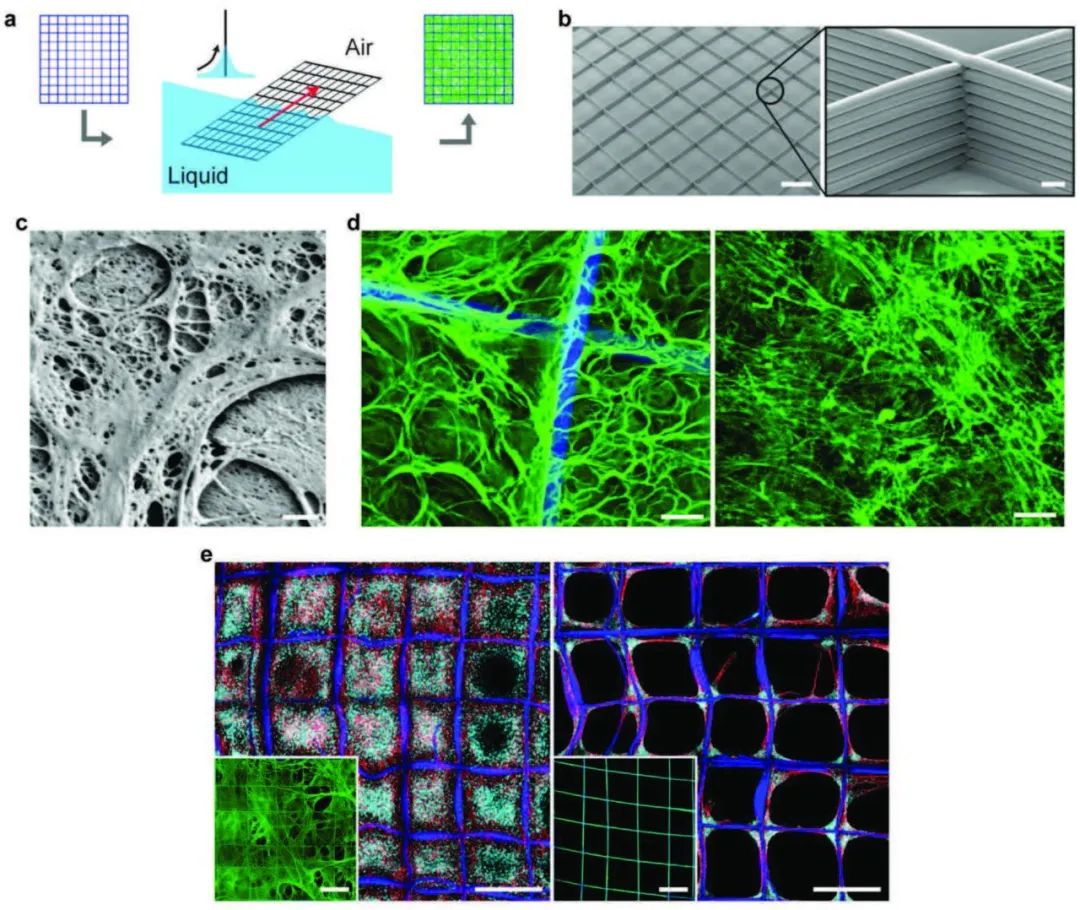
ͼ1. ˮ�����յ�Fnԭ��ά����
��������֧��������Fn��Һ�����ٶ�8ת/���ӣ����ڿ�����Fn��Һ��֧������Ӵ���λ��������Һ״̬��fFn���磬��������û��ʹ�ñ��Լ���ͼ1����֧������3D jet writing[2]������ӡPLGA��ã�����500x500um���οף����120um����Ϊϸ�������������ṩ������������������ʡ����������fFn������������άĸϸ�������Ļ��ʵ���̬���ơ�
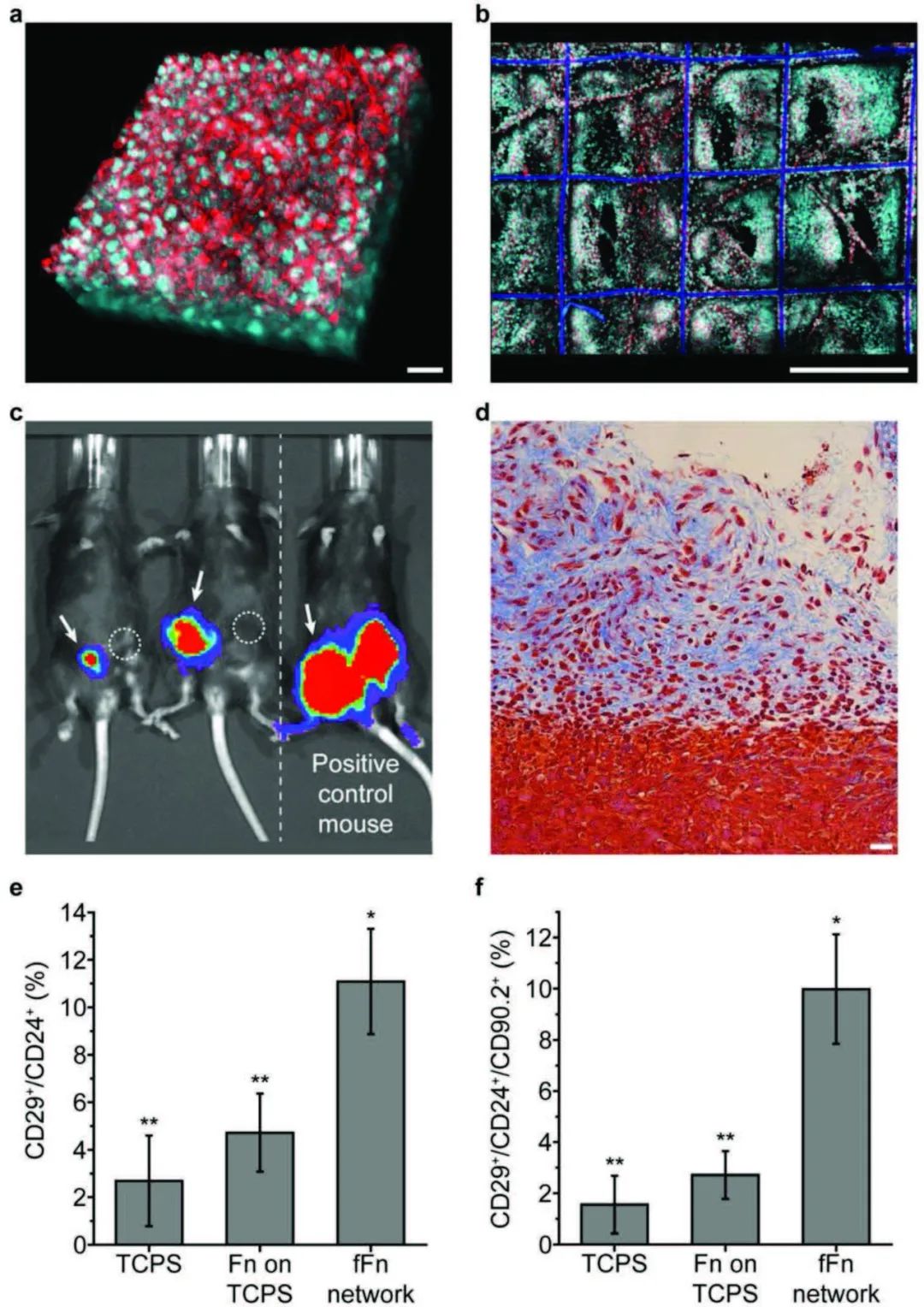
ͼ2. fFn�������������ٰ�ģ��������������ֲЧ��
����FnΪԭ�������ٰ�ϸ������ʵ���Ҫ�ɷ֣����߲�����fFn�������������ٰ�ģ��������������ֲЧ�ʵ�������ͼ2�������ȣ�������֧����������AT-3С�����ٰ�ϸ��������ϸ������fFn�������ȶ�����ө���ӫ����ø�������30000ϸ����fFn֧�ܱ�ֲ��������C57BL/6��������Ź����ͼƬ��ʾ����֧���У���ʼ�����������ź���ֲ����������֡��෴����ϸ����Һ�о���21��Ҳδ������������ֲ����ֲ��������֯ѧͼƬ��ʾ����ϸ������fFn������������Χ��֯����������������������Խ��һ�£�fFn�����е�AT-3ϸ��������������ʼ��Ⱥ��CD29+/CD24+����ת�ƣ�CD29+/CD24+/CD90.2+����
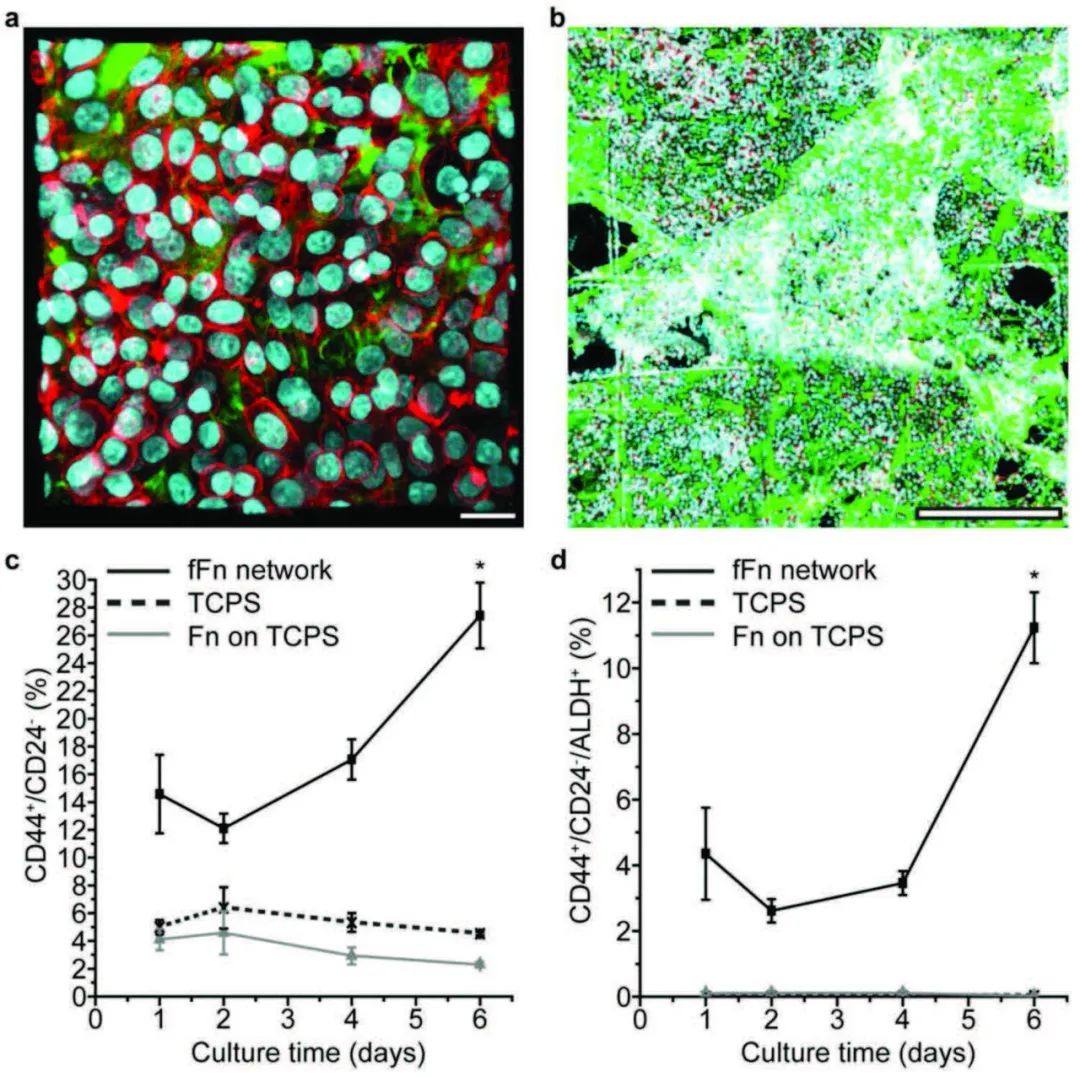
ͼ3. fFn��������MDA-MB-468�������ٰ�ϸ����������ʼϸ����
��������ֲ�����fFn�������������������ٰ�ϸ�����Ƿ�Ҳ�����������ԡ�ѡ����MDA-MB-468ϸ��ϵ�У�ͼ3�������������֮��MDA-MB-468ϸ���γ�����չ����ﵽ10ƽ����������3D��֢����������������֯�����۱���ϩ��TCPS���ϣ���FnͿ����TCPS�ϵ�ϸ����ȣ�fFn�����ϵ�CD44+/CD24−��Ⱥ��������ǰ���ߡ��������⣬������ʱ����ϣ�fFn�����ϵ�CD44+/CD24−/ALDH+��ȺҲ���������ڿ�����ġ�MDA-MB-468ϸ������4��֮��fFn���类ȥϸ�����������Fn�Ͳ�������Ⱦɫ�����֤��MDA-MB-468ϸ��ֻ�Ƿ����������IJ������ף���ԭ����fFn���绹�DZ�����á�֤��Fn��������Ƥ����ת������ҪECM���ء�
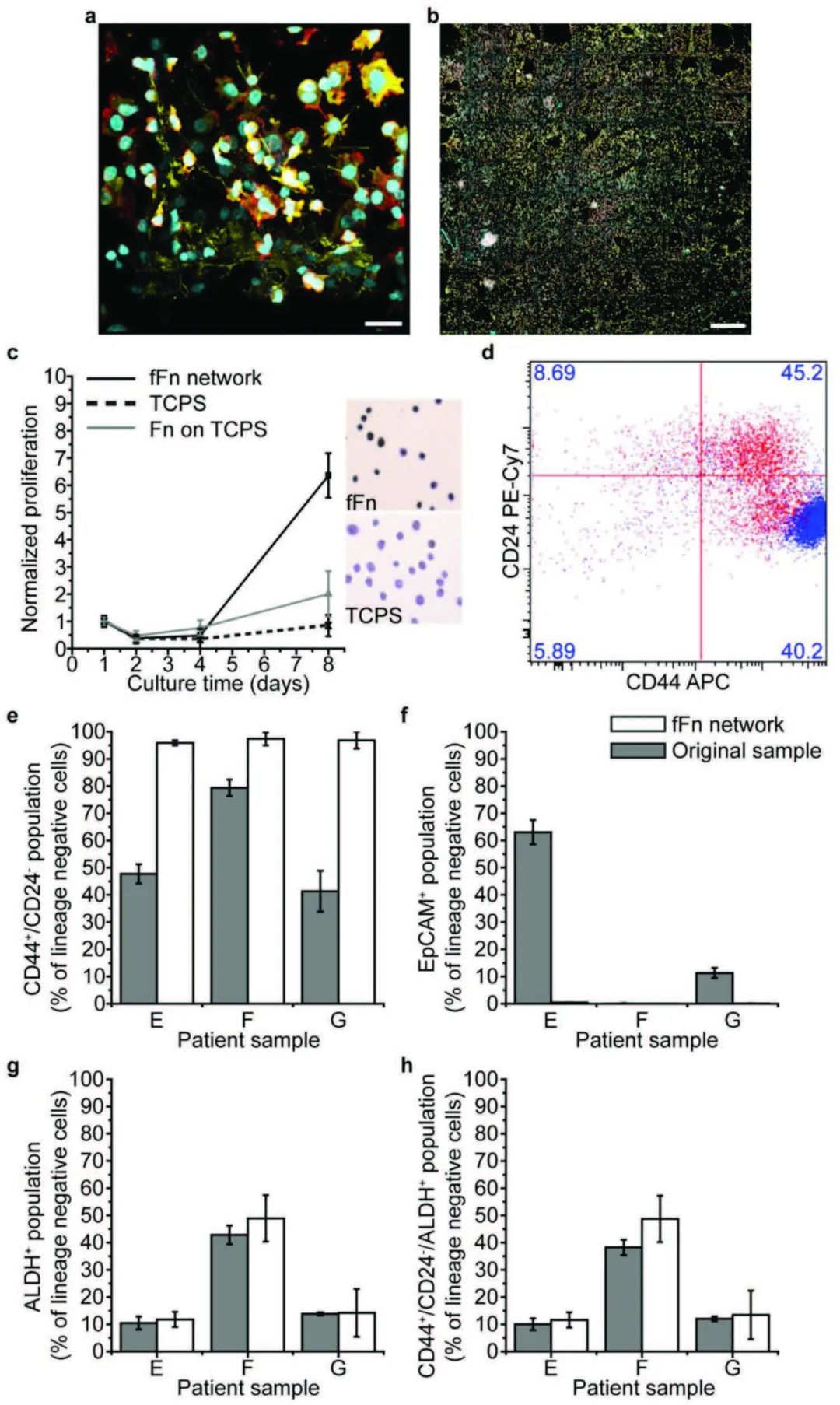
ͼ4. fFn���������������ٰ�ϸ��
������߲���������fFn����ֱ�������������ٰ�ϸ���������������ʾ8���ʱ��fFn֧�ܵ����������ȶ�����߳�7������fFn֧�ܿ����������յ����ٰ�����ϸ������Ƥ����ת����
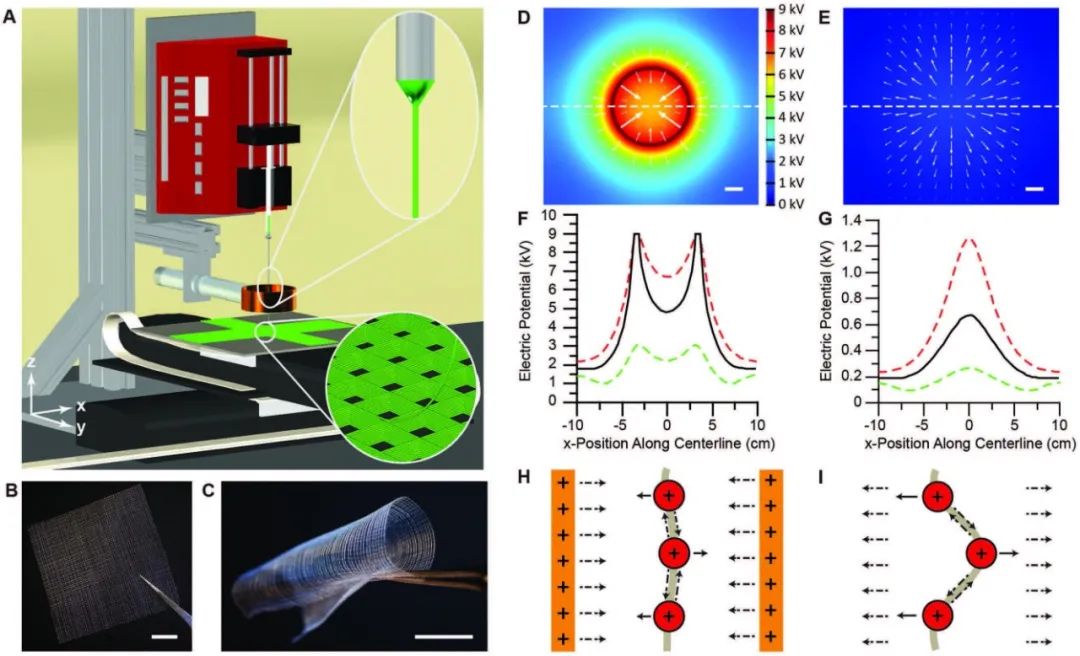
ͼ5. 3D jet writing
�����е�����״�ۺ���֧����Joerg Lahann�����Ŷ�֮ǰ�����3D Jet Writing�������죬���������2018�귢����Advanced Materials��־�ϣ���Ϊ3D jet writing: functional microtissues based ontessellated scaffold architectures���ù��յ��������ڿ���3ά�߾��ȵس����ۺ�����ά���Ҳ���Ҫ���������������¼��ȣ�Ϊ��ϸ���ĸ߾��ȵ�Ĵ�ӡ���»��������ص������ڴ�ӡ��ͷ�ĵײ���װ��һ�����缫����������ά�ڳ��������еIJ��ȶ����Ӷ�����ʵ�ָ��ظ����ȵĴ�ӡ��
�ο����ף�
[1] Jordahl S, Solorio L, Neale D B, et al. Engineered Fibrillar Fibronectin Networks as Three�\Dimensional Tissue Scaffolds[J]. Advanced Materials, 2019, 31(46): 1904580.
[2] Jordahl J H, Solorio L, Sun H, et al. 3D jet writing: functional microtissues based on tessellated scaffold architectures[J]. Advanced Materials, 2018, 30(14): 1707196.
(���α༭��admin)
��һƪ���������������Ա��3D��ӡ�������ºϽ�����ȡ��ͻ��
��һƪ���廪��ѧ���ݱ���������Ȼ˫����ˮ������������3D��ӡ�е�Ӧ��
��һƪ���廪��ѧ���ݱ���������Ȼ˫����ˮ������������3D��ӡ�е�Ӧ��
��������
- ��ȫ3D��ӡ����+�ɽ���ܣ�����뵼��
- ������3D��ӡ���ɿ��ٽ���̼��ά���ӻ��
- ���й������ڶ����̾�ȡ�����ͽ����벻��
- ����һɽ�����ݶ����������û�ȫ����
- ����ʮ�˹���һ�仨����һ�����Ф������
- ��������������������������������
- ������ɽ��ˮ����һ�����Ф�����������
- ����С����ѵ���ɣ����������ӵܡ���
- ��������������һ�����Ф�����������
- �����Ź���ϲ����ʲô��Ф�����������ʵ
�ȵ�����
- ������������ϲ��꣬���º�˳һ�Ÿ�����
- �������˿���һ�߸�����һ��ȷ��Ф������
- �����˶�֮�š���һ��ȷ��Ф�����������
- �����������������룬һ����ɫ����һ����
- ����С�Ŵ��á���ʲô��Ф������ʵ
- ����������֪����һ�����Ф��������
- �����������Ҳ��������ȳ����
- ����ɽ��������㡱��һ�����Ф���
- ��������Գ���뻢������ʲô��Ф�������
- ����������ս����һ���ȷ��Ф�����


 Conflux Technology ��110
Conflux Technology ��110 ͨ��������Forge NanoͶ��
ͨ��������Forge NanoͶ�� ���пƼ���ѧ����������Si
���пƼ���ѧ����������Si ����������ҽ�Ƶ���ҵ��TP
����������ҽ�Ƶ���ҵ��TP Amnovis����3D��ӡ������
Amnovis����3D��ӡ������ ����������ά3D��ӡ����
����������ά3D��ӡ���� ������ά2023ȫ��
������ά2023ȫ�� �Ϻ�����ȹ�ӭ��
�Ϻ�����ȹ�ӭ�� 3D��ӡ����ֲ����
3D��ӡ����ֲ���� FRI����֬�Ͱ�ˮ
FRI����֬�Ͱ�ˮ ������ۺ��Ⱦ��
������ۺ��Ⱦ�� ���һƬ�������
���һƬ�������

